2190 - EFICACIA Y SEGURIDAD DEL TRATAMIENTO ANTIRRETROVIRAL INYECTABLE DE ACCIÓN PROLONGADA (CABOTEGRAVIR/RILPIVIRINA) Y COMPARACIÓN ENTRE SEXOS
Medicina Interna, Hospital Arnau de Vilanova de Lleida, Lleida, España.
Objetivos: Describir las características de pacientes VIH en tratamiento antirretroviral (TAR) con cabotegravir/rilpivirina intramuscular de acción prolongada (Long Acting) en una Unidad de VIH, evaluar su eficacia y seguridad, y determinar si existen diferencias entre sexos.
Métodos: Se revisaron las historias clínicas de los pacientes VIH que iniciaron TAR con long acting en nuestra Unidad entre abril de 2023 y 2025. Para su prescripción, fue criterio ineludible haber descartado coinfección por VHB y VIH-1 subtipo A6/A1, así como mantener buena adherencia terapéutica, con supresión virológica durante un mínimo de 6 meses. Se recogieron los siguientes datos: edad, género, procedencia geográfica, orientación sexual, vía de transmisión, hábitos tóxicos, relaciones sexuales de riesgo; año, LTCD4 y carga viral al diagnóstico, TAR previos, adherencia, subtipo de VIH-1 y estudio basal de resistencias. Durante el seguimiento, se realizaron controles antropométricos y analíticos incluyendo perfil lipídico, glicémico, inmunovirológico con LTCD4 y carga viral. Se realizó un análisis de muestras apareadas mediante Jamovi. Este estudio fue aprobado por el CEIC de nuestro centro.
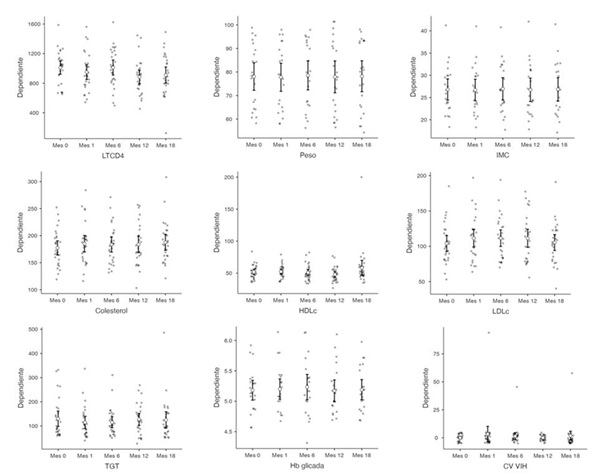
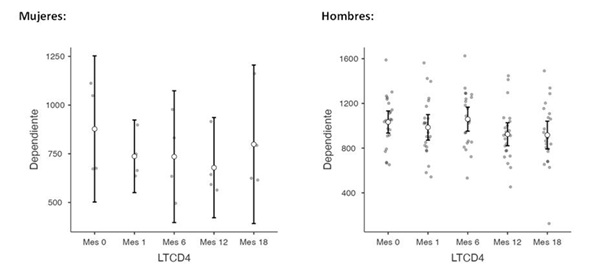
Resultados: De 73 pacientes en long acting, 80,8% fueron varones, con una edad media de 39 años y procedentes de España (67%), seguido de Sudamérica (23,3%) y África (5,4%). Destaca el largo tiempo de evolución desde el diagnóstico de VIH, entre 1992 y 2003, con una media de CD4 nadir de 449. Habían recibido entre 2 y 5 TAR previos al switch a long acting, siendo los regímenes provenientes más frecuentes bictegravir/emtricitabina/tenofovir alafenamida (68,5%) y dolutegravir/lamivudina (18,8%). El principal subtipo de VIH-1 fue el B (35,6%) y se descartó la presencia de mutaciones mayores en la mayoría de casos (63%). En un 27% se inició el TAR sin disponer de genotipado; a ello se atribuyeron los dos únicos fracasos terapéuticos, presentando un paciente 1631 copias/ml al control del año, con desarrollo de resistencias a no análogos de la transcriptasa inversa e inhibidores de la integrasa, y el otro, 168 copias/ml al mes de tratamiento (descartado blip). En ambos se utilizó bictegravir/emtricitabina/tenofovir alafenamida como pauta de rescate, recuperando supresión virológica. La carga viral se mantuvo indetectable en todo momento en el resto de pacientes (97,21%). No se observó impacto clínicamente relevante en el control inmunitario (descenso estadísticamente significativo en el recuento de CD4 (tabla 1 y figura 1), aunque manteniéndose por encima de 600 copias en todo momento). Además, se perdió la significación estadística al realizar el análisis por sexos (tabla 2 y figura 2). Respecto al seguimiento, no se observó empeoramiento del perfil lipídico, glicémico, ni aumento ponderal tras el inicio del long acting. El principal efecto adverso fue dolor leve en la zona de punción (82%).
|
Tabla 1. Recuento total de CD4, peso, IMC, colesterol total, colesterol HDL, colesterol LDL, triglicéridos totales, hemoglobina glicosilada y carga viral del VIH |
|||||
|
Efectos dentro de los sujetos |
|||||
|
|
Suma de cuadrados |
gl |
Media cuadrática |
F |
p |
|
LTCD4 |
375499 |
4 |
93875 |
2,66 |
0,037 |
|
Peso |
7,39 |
4 |
1,85 |
0,353 |
0,841 |
|
IMC |
1,03 |
4 |
0,258 |
0,418 |
0,795 |
|
ColT |
1600 |
4 |
400 |
0,747 |
0,562 |
|
HDLc |
1639 |
4 |
410 |
2,1 |
0,085 |
|
LDLc |
1556 |
4 |
389 |
0,806 |
0,524 |
|
TGT |
5728 |
4 |
1432 |
0,74 |
0,566 |
|
HbA1c |
0,0476 |
4 |
0,0119 |
0,383 |
0,82 |
|
CV VIH |
225 |
4 |
56,1 |
0,576 |
0,68 |
|
Suma de Cuadrados Tipo 3 |
|
Tabla 2.1. Medias marginales estimadas LTCD4 en ambos sexos |
||||||||
|
Intervalo de confianza al 95% |
||||||||
|
|
Media |
EE |
Inferior |
Superior |
||||
|
LTCD4 |
Mujeres |
Hombres |
Mujeres |
Hombres |
Mujeres |
Hombres |
Mujeres |
Hombres |
|
Mes 0 |
878 |
1034 |
117,9 |
55,1 |
502 |
935 |
1253 |
1133 |
|
Mes 1 |
737 |
986 |
58,6 |
51,8 |
550 |
871 |
924 |
1100 |
|
Mes 6 |
735 |
1059 |
106,3 |
49,5 |
397 |
952 |
1074 |
1167 |
|
Mes 12 |
679 |
924 |
80,8 |
60,0 |
421 |
822 |
936 |
1027 |
|
Mes 18 |
799 |
917 |
127,9 |
55,1 |
392 |
792 |
1206 |
1041 |
|
Tabla 2.2. Comparaciones post hoc LTCD4 en mujeres |
||||||
|
Comparación |
|
|||||
|
LTCD4 |
LTCD4 |
Diferencia de medias |
EE |
gl |
t |
p |
|
Mes 0 |
Mes 1 |
140,5 |
80,5 |
3 |
1,7455 |
0,179 |
|
Mes 6 |
142,25 |
54,4 |
3 |
2,6149 |
0,079 |
|
|
Mes 12 |
198,75 |
90,4 |
3 |
2,1989 |
0,115 |
|
|
Mes 18 |
78,75 |
63,8 |
3 |
1,2344 |
0,305 |
|
|
Mes 1 |
Mes 6 |
1,75 |
53,4 |
3 |
0,0328 |
0,976 |
|
Mes 12 |
58,25 |
28,9 |
3 |
2,0182 |
0,137 |
|
|
Mes 18 |
-61,75 |
118,9 |
3 |
-0,5194 |
0,639 |
|
|
Mes 6 |
Mes 12 |
56,5 |
58,3 |
3 |
0,9687 |
0,404 |
|
Mes 18 |
-63,5 |
109,3 |
3 |
-0,5809 |
0,602 |
|
|
Mes 12 |
Mes 18 |
-120 |
138,2 |
3 |
-0,868 |
0,449 |
|
Tabla 2.3. Comparaciones post hoc LTCD4 en varones |
||||||
|
Comparación |
||||||
|
LTCD4 |
LTCD4 |
Diferencia de medias |
EE |
gl |
t |
p |
|
Mes 0 |
Mes 1 |
48,04 |
46,3 |
22 |
1,039 |
0,31 |
|
Mes 6 |
-25,65 |
51,1 |
22 |
-0,502 |
0,62 |
|
|
Mes 12 |
109,48 |
64,7 |
22 |
1,693 |
0,105 |
|
|
Mes 18 |
116,87 |
58,4 |
22 |
2 |
0,058 |
|
|
Mes 1 |
Mes 6 |
-73,7 |
51,6 |
22 |
-1,427 |
0,168 |
|
Mes 12 |
61,43 |
60,3 |
22 |
1,019 |
0,319 |
|
|
Mes 18 |
68,83 |
64,5 |
22 |
1,067 |
0,298 |
|
|
Mes 6 |
Mes 12 |
135,13 |
45,2 |
22 |
2,992 |
0,007 |
|
Mes 18 |
142,52 |
64,9 |
22 |
2,196 |
0,039 |
|
|
Mes 12 |
Mes 18 |
7,39 |
72,4 |
22 |
0,102 |
0,92 |
Conclusiones: El TAR con cabotegravir/rilpivirina intramuscular bimestral ha demostrado eficacia y seguridad, manteniendo supresión virológica en pacientes seleccionados, sin impacto en el control lipídico, glicémico ni ponderal. No se observaron diferencias estadísticamente significativas entre hombres y mujeres. Es importante disponer de genotipado para evitar fracasos virológicos y desarrollo de resistencias.







