1359 - EFICACIA Y SEGURIDAD DE LOS INMUNOSUPRESORES EN EL TRATAMIENTO DE LA ARTERITIS DE CÉLULAS GIGANTES
1Medicina Interna, Hospital Gregorio Marañón, Madrid, España. 2Medicina Interna, Hospital Puerta de Hierro, Majadahonda, España. 3Medicina Interna, Fundación Jiménez Díaz, Madrid, España. 4Medicina Interna, Hospital Ramón y Cajal, Madrid, España. 5Medicina Interna, Hospital Infanta Cristina, Madrid, España.
Objetivos: Describir la eficacia y seguridad de los inmunosupresores en el tratamiento de pacientes con arteritis de células gigantes (ACG).
Métodos: Estudio multicéntrico, observacional, retrospectivo de una cohorte de 154 pacientes diagnosticados de ACG según los criterios de la EULAR 2022. Los pacientes se estratificaron en función del régimen terapéutico recibido en 4 grupos: monoterapia con corticoides, metotrexato (MTX), tocilizumab (TCZ) y tratamiento inmunosupresor (IS) combinado. Se compararon las variables epidemiológicas, demográficas, clínicas, el tratamiento de inducción y los desenlaces en cada grupo. El objetivo primario (porcentaje de pacientes con enfermedad activa) y los objetivos secundarios (remisión sin esteroide, dosis basal de prednisona, dosis acumulada de esteroide, efectos adversos de esteroides, complicaciones infecciosas y complicaciones de tratamiento) se determinaron a los 12 y 36 meses del inicio de tratamiento.
Resultados: Se analizaron 154 pacientes con ACG. Entre las características de la población en los distintos grupos de tratamiento (tabla) no hubo diferencias significativas salvo por un mayor número de pacientes con osteoporosis en el grupo de pacientes tratados con TCZ (40%) frente al grupo de monoterapia con corticoides y al grupo de MTX (13,5% y 16,3% respectivamente, p < 0,05). Por otro lado, los pacientes tratados con inmunosupresores presentaron más cefalea que el grupo de monoterapia (71,7% MTX y 71,2% IS combinado vs. 48,4%, p < 0,05) y los tratados con TCZ tuvieron una presencia significativamente mayor de polimialgia reumática (60% frente a 30,5% en el grupo de monoterapia y 34,8% en grupo MTX) y de afectación extracraneal (46,7 vs. 15,8% y 15,2%). En las figuras 1 y 2 se muestran los objetivos primarios y secundarios. En relación con el objetivo primario, y aunque no hubo diferencias estadísticamente significativas, el grupo de pacientes con IS tenía un porcentaje de enfermedad activa de 3,4% a los 12 meses y de 5,1% a los 36 meses, en comparación con el grupo tratado con esteroide en monoterapia (9,5% y 5,3%, respectivamente). A los 12 meses, el grupo IS, a expensas de MTX, tenían una menor dosis basal de prednisona en relación con el grupo de monoterapia (4,4 mg vs. 6,4 mg, p < 0,05). Asimismo, la dosis acumulada de esteroide a los 12 meses para MTX (1.250,5 mg), TCZ (969,2 mg) y los IS combinados (1.207,1 mg) fue menor en comparación con el grupo control (1.983,62 mg, p < 0,05). Esta diferencia se mantuvo a los 36 meses para el grupo MTX (614,1 mg) e IS combinado (582,1 mg), frente al grupo de monoterapia (1.380,5 mg, p < 0,05). No se identificaron diferencias con la proporción de pacientes en remisión sin esteroide, en los efectos adversos por esteroides o en la tasa de complicaciones infecciosas o del tratamiento.
|
Características de la población |
|||||
|
|
General (n = 154) |
Monoterapia (n = 95) |
MTX (n = 46) |
TCZ (n = 15) |
MTX/TCZ (n = 59) |
|
Edad (años) (media, DE) |
74,75 (15,41) |
74,1 (16,9) |
75,1 (14,1) |
75,8 (8,51) |
75,4 (12,9) |
|
Sexo femenino (n, %) |
98 (63,6) |
60 (63,2) |
27 (58,7) |
12 (80) |
38 (64,4) |
|
Etnia caucásica (n, %) |
149 (96,8) |
91 (95,8) |
45 (97,8) |
15 (100) |
58 (98,3) |
|
HTA (n, %) |
99 (64,2) |
61 (65,6) |
30 (65,2) |
9 (60) |
38 (64,4) |
|
DM (n, %) |
36 (23,3) |
23 (24,7) |
8 (17,8) |
6 (40) |
13 (22,4) |
|
DL (n, %) |
69 (44,8) |
42 (44,2) |
21 (45,7) |
7 (46,7) |
27 (45,8) |
|
Obesidad (n, %) |
13 (8,4) |
10 (11,4) |
2 (4,4) |
1 (6,7) |
3 (5,2) |
|
Tabaco (n, %) |
15 (9,7) |
10 (10,5) |
4 (8,7) |
2 (13,3) |
5 (8,5) |
|
Osteoporosis previa (n, %) |
24 (15,6) |
12 (13,5) |
7 (16,3) |
6 (40)* |
12 (21,4) |
|
Características clínicas de la enfermedad |
|||||
|
Síntomas/Signos (n, %) |
|||||
|
Cefalea |
88 (57,1) |
46 (48,4)* |
33 (71,7)* |
10 (66,7) |
42 (71,2)* |
|
Claudicación mandibular |
41 (26,6) |
24 (25,3) |
13 (28,3) |
5 (33,3) |
17 (28,8) |
|
Constitucional |
82 (53,2) |
54 (56,8) |
22 (47,8) |
8 (53,3) |
28 (47,5) |
|
Fiebre |
51 (33,1) |
36 (37,9) |
12 (26,1) |
4 (26,7) |
15 (25,4) |
|
PMR |
53 (34,4) |
29 (30,5) |
16 (34,8) |
9 (60)* |
24 (40,7) |
|
Territorio (n, %) |
|||||
|
Craneal |
89 (57,8) |
54 (56,8) |
27 (58,7) |
9 (60) |
35 (59,3) |
|
Extracraneal |
28 (18,2) |
15 (15,8) |
7 (15,2) |
7 (46,7)* |
13 (22) |
|
Aorta |
30 (19,5) |
18 (18,9) |
7 (15,2) |
6 (40)* |
12 (20,33) |
|
Axilar bilateral |
9 (5,8) |
3 (3,2) |
3 (6,5) |
4 (26,7)* |
6 (10,2) |
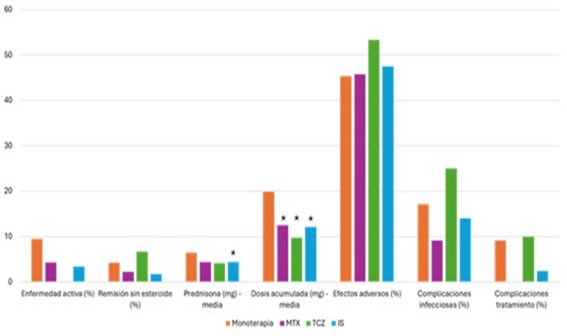
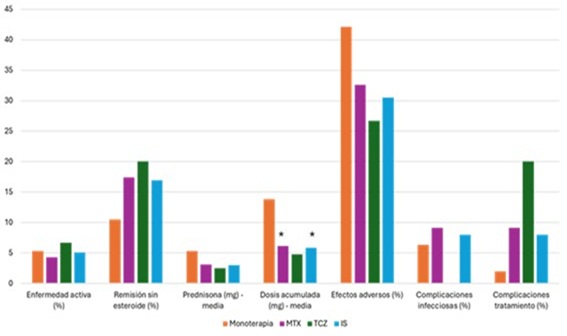
Conclusiones: El uso de inmunosupresores asocia un ahorro de corticoides a medio y largo plazo con una tendencia a mayor tasa de remisión y sin un peor perfil de seguridad, invitando a su uso en pacientes con mayor riesgo de efectos secundarios por corticoides.







