154 - ARTERITIS DE CÉLULAS GIGANTES: ESTUDIO DESCRIPTIVO Y ANÁLISIS DE CONGLOMERADOS
1Medicina Interna, Hospital Clínico Universitario de Valladolid, Valladolid, España. 2Radiodiagnóstico, Hospital Clínico Universitario de Valladolid, Valladolid, España.
Objetivos: Describir las presentaciones clínicas de la arteritis de células gigantes (ACG) y analizar perfiles de pacientes mediante técnicas de agrupamiento según el debut, así como tratamiento inicial y la evolución.
Métodos: Estudio de cohortes retrospectivo de pacientes con ACG atendidos en la unidad de Enfermedades Autoinmunes Sistémicas de un hospital terciario entre enero de 2020 y diciembre de 2024. Se excluyeron aquellos pacientes en los que no se pudo obtener datos sobre su debut, tratamiento o con pérdida del seguimiento. Se recogieron variables epidemiológicas, clínicas, analíticas, terapéuticas y evolutivas (recaídas, efectos adversos). Se realizó análisis de conglomerados jerárquico (método de Ward) y posteriormente K-medias, basados en los datos del debut, y se evaluó su evolución.
Resultados: Tras excluir 6 pacientes, se incluyeron 44 casos. 32 (72,7%) eran mujeres, con una media de edad de 74,2 años (desviación estándar (DE) 8,3). Los síntomas más frecuentes al debut fueron los craneales (36 pacientes, 81,8%) seguidos de la polimialgia reumática (22, 50,0%). En el análisis por conglomerados, se utilizó el método jerárquico y se optó por 3 como número de conglomerados (fig. 1). Posteriormente, se realizó un análisis de K-medias con tres conglomerados, observándose correlación aceptable entre ambos resultados. La presentación al debut se muestra en la tabla 1. El 46% de los pacientes recibieron bolos de corticoides. La dosis inicial de prednisona fue de 46,7 mg/día (DE 14,7). Se asociaron inmunosupresores (IS) al diagnóstico en el 64% de los pacientes. El 55% de los pacientes recayeron y el 15% presentó infecciones graves durante el seguimiento. Los datos respecto al tratamiento y la evolución se recogen en la tabla 2 y figura 2.
|
Tabla 1 |
|||||
|
Serie global (n = 44) |
Conglomerado 1 (n = 11) |
Conglomerado 2 (n = 23) |
Conglomerado 3 (n = 10) |
p |
|
|
Edad años (DE) |
74,2 (8,3) |
76,3 (8,8) |
77,4 (6,0) |
64,7 (5,1) |
< 0,001 |
|
Sexo femenino n (%) |
32 (72,7) |
9 (81,8) |
14 (60,9) |
9 (90,0) |
0,166 |
|
Debut craneal n (%) |
36 (81,8) |
11 (100,0) |
22 (95,7) |
3 (30,0) |
< 0,001 |
|
Debut isquémico n (%) |
18 (40,9) |
1 (9,1) |
14 (60,9) |
3 (30,0) |
0,012 |
|
Síntomas sistémicos n (%) |
18 (40,9) |
11 (100,0) |
2 (8,7) |
5 (50,0) |
< 0,001 |
|
Polimialgia reumática n (%) |
22 (50,0) |
5 (45,5) |
10 (43,5) |
7 (70,0) |
0,353 |
|
VSG mm/h (DE) |
75,9 (30,1) |
99,5 (15,7) |
67,0 (25,4) |
70,6 (39,6) |
0,008 |
|
PCR mg/L (DE) |
83,15 (65,70) |
144,85 (69,82) |
59,69 (48,38) |
69,24 (56,69) |
< 0,001 |
|
Hemoglobina g/dL (DE) |
11,9 (1,9) |
11,0 (1,3) |
12,1 (2,1) |
12,2 (1,9) |
0,225 |
|
Tabla 2 |
|||||
|
Serie global (n = 44) |
Conglomerado 1 (n = 11) |
Conglomerado 2 (n = 23) |
Conglomerado 3 (n = 10) |
p |
|
|
Uso de bolos de GC n (%) |
20 (45,5) |
2 (18,2) |
13 (56,5) |
5 (50,0) |
0,104 |
|
Dosis inicial de prednisona o equivalentes mg (DE) |
46,7 (14,7) |
45,9 (14,3) |
46,5 (15,3) |
48,0 (15,5) |
0,948 |
|
Tratamiento con IS al diagnóstico (MTX, TCZ) n (%): |
28 (63,6) |
8 (72,7) |
12 (52,2) |
8 (80,0) |
0,240 |
|
Dosis acumulada de prednisona o equivalentes en 12 meses mg (DE) |
5.154,79 (2.580,44) |
4.239,15 (2.377,69) |
6.023,71 (2.651,45) |
4.163,45 (2.073,88) |
0,620 |
|
Suplementos de calcio y vitamina D n (%) |
38 (86,4) |
10 (90,9) |
19 (82,6) |
9 (90,0) |
0,748 |
|
Bifosfonatos n (%) |
29 (65,9) |
8 (72,7) |
14 (60,9) |
7 (70,0) |
0,755 |
|
Recaída (≥ 1) n (%) |
24 (54,5) |
6 (54,5) |
14 (60,9) |
4 (40,0) |
0,542 |
|
Infecciones (≥ 1) n (%): |
7 (15,9) |
2 (18,2) |
5 (21,7) |
0 (0,0) |
0,284 |
|
Infecciones graves |
4 |
0 |
4 |
0 |
|
|
Pneumocystis jirovecii |
1 |
1 |
0 |
0 |
|
|
Herpes zóster |
3 |
1 |
2 |
0 |
|
|
Efectos secundarios GC (≥ 1) n (%): |
17 (38,6) |
3 (27,3) |
22 (47,8) |
3 (30,0) |
0,420 |
|
Osteoporosis complicada |
6 |
3 |
3 |
0 |
|
|
Catarata |
10 |
0 |
8 |
2 |
|
|
Evento cardiovascular |
5 |
0 |
4 |
1 |
|
|
Tiempo de tratamiento meses (DE) |
35,9 (19,6) |
35,3 (21,1) |
38,8 (18,7) |
30,1 (20,7) |
0,510 |
|
Tiempo de tratamiento inmunosupresor meses (DE) |
26,5 (22,3) |
30,9 (22,8) |
24,0 (23,5) |
27,1 (20,2) |
0,709 |
|
Tiempo de seguimiento meses (DE) |
39,5 (21,0) |
38,0 (22,6) |
44,0 (19,7) |
31,0 (21,6) |
0,262 |

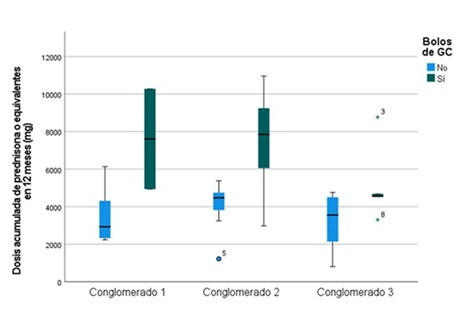
Discusión: Se identificaron tres perfiles clínicos al diagnóstico. El primer conglomerado agrupó a mujeres, de edad avanzada, con síntomas sistémicos y craneales, así como alteraciones analíticas marcadas. El uso de IS desde el inicio fue elevado, consiguiéndose un importante ahorro de corticoides a 12 meses sin mayores tasas de recidivas. Pese a ello, un tercio desarrolló fracturas osteoporóticas. El segundo integra los pacientes más ancianos y con mayor porcentaje de varones. Muestran un perfil analítico más anodino, destacando el gran porcentaje de debut isquémico. Esto explica que en más de la mitad de los casos se indicaran bolos de corticoides. Fue el grupo que recibió más corticoides en monoterapia y con mayor dosis acumulada en 12 meses. Asimismo, presentó la mayor tasa de recaídas, infecciones, eventos cardiovasculares y cataratas. El último grupo fue el más joven, con más polimialgia reumática al debut y menos sintomatología craneal. La inmunosupresión se indicó ampliamente, consiguiéndose ahorro de corticoides y la menor tasa de recaídas, en ausencia de infecciones graves.
Conclusiones: El análisis por conglomerados en la ACG permite identificar perfiles clínicos diferenciados, siendo de utilidad para orientar la terapéutica inicial y predecir la evolución.
Bibliografía
1. Hellmich B, Agueda A, Monti S, Buttgereit F, de Boysson H, Brouwer E, et al. 2018 Update of the EULAR recommendations for the management of large vessel vasculitis. Annals of the Rheumatic Diseases. 2020;79(1):19-30.







