1456 - RESULTADOS DEL ENSAYO CLÍNICO ALEATORIZADO PROTHROMCOVID: SUBANÁLISIS EN FUNCIÓN DEL ESTADO DE VACUNACIÓN
1Hospital Universitario Infanta Leonor, Madrid. 2Hospital Clínic, Barcelona. 3Hospital de Emergencias Enfermera Isabel Zendal, Madrid. 4Hospital Virgen de la Luz, Cuenca. 5Hospital Clínico San Carlos, Madrid. 6Hospital Universitario de Vinalopó, Elche (Alicante).
Objetivos: Evaluar la eficacia y la seguridad de la tinzaparina en dosis profilácticas, intermedias y terapéuticas en pacientes no críticos ingresados por neumonía por COVID-19 (PROTHROMCOVID trial), Evaluar si existen diferencias en función del estado de vacunación de los pacientes.
Métodos: Ensayo aleatorizado controlado y multicéntrico (PROTHROMCOVID) que incluyó a pacientes adultos hospitalizados no críticos con neumonía por COVID-19 en 18 centros españoles desde el 1 de febrero al 30 de septiembre 2021. Intervención: Los pacientes eran incluidos con al menos uno de los siguientes criterios: Sat O2 150 mg/L-IL6 > 40 pg/mL. Fueron aleatorizados a dosis profilácticas (4.500 UI), intermedias (100 UI/kg) o terapéuticas (175 UI/kg) de tinzaparina durante la hospitalización, seguidas de 7 días de tinzaparina profiláctica al alta. La variable principal de eficacia es una variable combinada de eventos trombóticos sistémicos sintomáticos, necesidad de ventilación mecánica invasiva o no invasiva o muerte dentro de los primeros 30 días. La variable principal de seguridad se evaluó mediante hemorragia mayor los 30 días. Se registró el estado de vacunación de los pacientes ingresados. El ensayo se llevó a cabo de acuerdo con la Declaración de Helsinki y los requisitos reglamentarios locales. El protocolo fue aprobado por los comités éticos para la investigación en medicamentos del Hospital General Universitario Gregorio Marañón y todos los comités locales y la AEMPS. Todos los pacientes firmaron consentimiento informado.
Resultados: Se presentan los resultados del análisis intermedio preespecificado al 50% del tamaño muestral. 300 pacientes fueron incluidos en el análisis (edad media [DE], 56,7 [14,6] años; hombres, 182 [60,7%]. Las características basales fueron similares en los 3 grupos, incluyendo el dímero D, IL6, PCR y valores de ferritina. El tratamiento para la COVID-19 con corticosteroides (89,3%), remdesivir (18,0%) o tocilizumab (14,3%) fue comparable en los 3 grupos. El porcentaje de sujetos vacunados contra la COVID-19 fue del 16%, 29% y 26% en los grupos de profilaxis, dosis intermedias y terapéuticas de tinzaparina, respectivamente (p = 0,06). La variable principal a los 30 días de la aleatorización ocurrió en 58 pacientes (19,3%) de la población total; 19 (17,1%) en el grupo de dosis profilácticas, 20 (22,1%) en el grupo de dosis intermedias y 19 (18,5%) en el grupo de dosis terapéuticas (p = 0,72). 17 pacientes (21,7%) tuvieron evento de entre los pacientes vacunados, 41 pacientes (18,7%) tuvieron evento de entre los no vacunados, p (0,55), No se registró ninguna hemorragia mayor, se observó hemorragia no mayor en el 3,7% de los pacientes, sin diferencias entre los 3 grupos.
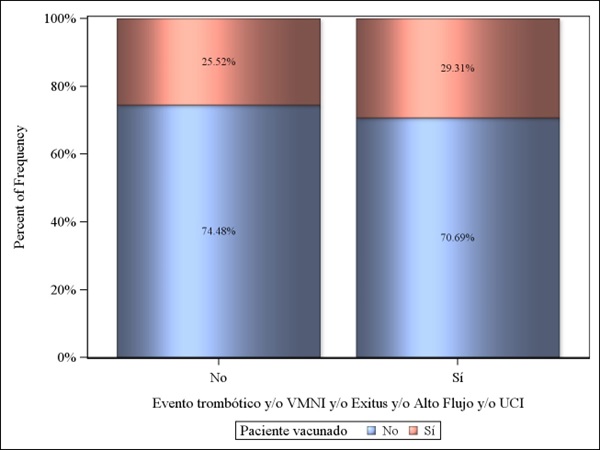
Conclusiones: En pacientes con neumonía COVID-19 no críticos, tanto en pacientes vacunados como en no vacunados, la tinzaparina a dosis intermedia o terapéutica en comparación con las dosis profilácticas estándar no parece aumentar el beneficio con respecto a la probabilidad de evento trombótico, ventilación invasiva o no invasiva o muerte tanto en pacientes NCT04730856.
Bibliografía
- The ATTACC, ACTIV-4a, and REMAP-CAP Investigators. Therapeutic Anticoagulation with Heparin in Noncritically Ill Patients with COVID-19. N Engl J Med. 2021;385(9):790-802.
- Casas-Rojo JM, Antón-Santos JM, Millán-Núñez-Cortés J, Lumbreras-Bermejo C, Ramos-Rincón JM, Roy-Vallejo E, et al. Clinical characteristics of patients hospitalized with COVID-19 in Spain: Results from the SEMI-COVID-19 Registry. Rev Clin Esp. 2020;220(8):480-94.






