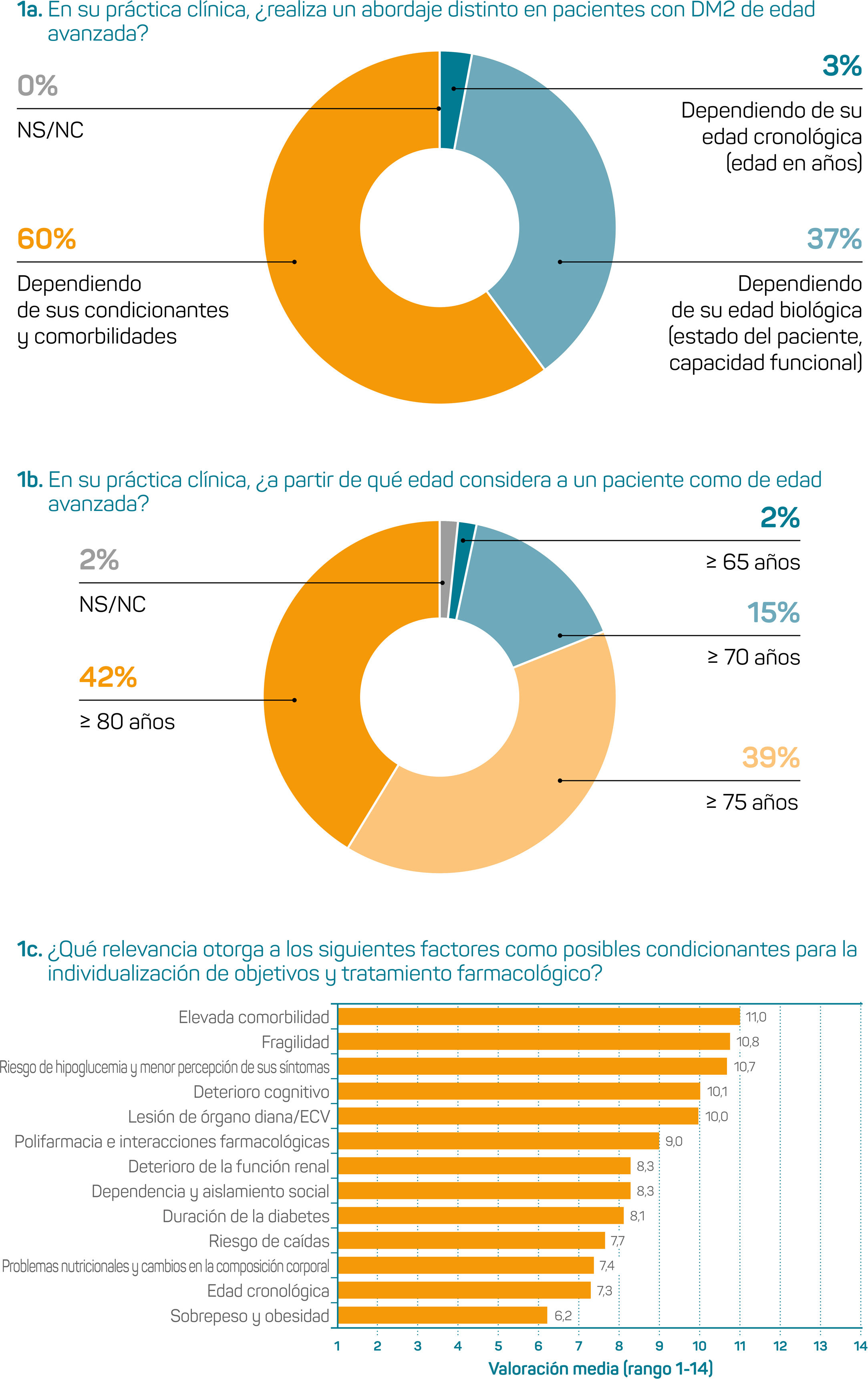
Explorar actitudes en la práctica clínica habitual de un grupo multidisciplinar de médicos en España en el manejo de pacientes de edad avanzada o frágiles con diabetes mellitus tipo 2.
MétodosSe utilizó una encuesta mixta tipo Delphi y preguntas de opinión, actitud y comportamiento. Se compararon las percepciones en atención primaria (n=211) y en atención hospitalaria (n=80).
ResultadosSe obtuvo consenso en todos los enunciados. El 87% de participantes consideró que los trastornos psiquiátricos graves condicionan el tratamiento antidiabético, y el 72% que la evaluación psicocognitiva es tan relevante como la del resto de comorbilidades. Los médicos de atención hospitalaria consideraron con mayor frecuencia que la comorbilidad afecta al autocuidado (95,0% vs. 82,9%), que la ausencia de desintensificación es una forma de inercia terapéutica (88,8% vs. 76,3%), que clasificar al adulto mayor como frágil es fundamental para elegir objetivos (96,3% vs. 87,7%), que debe valorarse la desintensificación del tratamiento antidiabético y el control de factores de riesgo cardiovascular en mayores de 80 años (90,0% vs. 78,7%) y que la diabetes mellitus tipo 2 predispone a la sarcopenia (86,3% vs. 71,6%). La utilidad de las guías clínicas fue más valorada entre los participantes de atención primaria (79,1% vs. 72,5%).
ConclusionesExisten aspectos susceptibles de mejora en el manejo de pacientes de edad avanzada o frágiles con diabetes mellitus tipo 2: la inercia en la desintensificación del tratamiento, la evaluación psicocognitiva o la identificación de fragilidad y sarcopenia.
This work aims to explore attitudes regarding the management of elderly or frail patients with type 2 diabetes mellitus in the routine clinical practice of a multidisciplinary group of physicians in Spain.
MethodsA mixed survey was used that included both Delphi and opinion, attitude, and behaviour (OAB) questions. Perceptions in primary care (n=211) and hospital care (n=80) were compared.
ResultsConsensus was obtained on all statements. Eighty-seven percent of participants considered that severe psychiatric disorders conditioned antidiabetic treatment and 72% that a psychocognitive assessment is as relevant as the assessment of other comorbidities. Hospital care physicians more frequently considered that comorbidity affects self-care (95.0% vs. 82.9%), that a lack of de-intensification is a form of therapeutic inertia (88.8% vs. 76.3%), that classifying older adults as frail is fundamental to choosing targets (96.3% vs. 87.7%), that de-intensification of antidiabetic treatment and control of cardiovascular risk factors should be considered in those over 80 years of age (90.0% vs. 78.7%), and that type 2 diabetes mellitus predisposes patients to sarcopenia (86.3% vs. 71.6%). The usefulness of clinical guidelines was more highly valued among primary care participants (79.1% vs. 72.5%).
ConclusionsThere is room for improvement on several aspects of managing elderly or frail patients with type 2 diabetes mellitus, including inertia in treatment de-intensification, conducting a psychocognitive assessment, or the identification of frailty and sarcopenia.
Artículo
Diríjase desde aquí a la web de la >>>FESEMI<<< e inicie sesión mediante el formulario que se encuentra en la barra superior, pulsando sobre el candado.
Una vez autentificado, en la misma web de FESEMI, en el menú superior, elija la opción deseada.

>>>FESEMI<<<