99 - ETNIA Y SEXO EN EL DAÑO RENAL Y ARTERIAL MEDIADOS POR HIPERTENSIÓN: ANÁLISIS INTERSECCIONAL EN PACIENTES HIPERTENSOS DEL SUR DE LONDRES
1Institut d'Investigació Germans Trias i Pujol, Badalona, España. 2University of Bremen, Bremen, Alemania. 3King's College London, London, Reino Unido.
Objetivos: Las personas de origen africano (OA) y las mujeres podrían tener mayor riesgo de daño renal y arterial mediado por hipertensión arterial (HTA). Sin embargo, la evidencia no es clara, pudiendo explicarse por confusores. El objetivo es analizar diferencias étnicas (OA y caucásico) y por sexo en el daño renal y arterial de pacientes hipertensos.
Métodos: Estudio transversal de pacientes hipertensos que atienden a la clínica de HTA de un hospital de tercer nivel de Londres entre 2017 y 2023. Los pacientes eran derivados desde atención primaria por debut de HTA a temprana edad o HTA de difícil control. Se recogieron variables antropométricas, antecedentes patológicos, factores de riesgo vascular, bioquímica sanguínea y urinaria, y velocidad de onda de pulso (VOP) mediante tonometría carótido-femoral. La muestra se dividió en 4 grupos interseccionales: mujeres caucásicas, hombres caucásicos, mujeres de OA y hombres de OA. Las diferencias entre grupos se analizaron mediante ANOVA (variables cuantitativas) o chi-cuadrado (variables categóricas). Se realizaron dos regresiones múltiples para ajustar por confusores: 1) Logística para la asociación con daño renal (filtrado glomerular < 60 mL/min y/o presencia de micro/macroalbuminuria); 2) Lineal para la asociación con la VOP (m/s). El estudio contó con la aprobación del Comité Ético de la institución.
Resultados: Se incluyeron 654 pacientes con HTA, de edad media de 46 años ± 13DE, de los cuales 163 eran mujeres de OA, 187 hombres de OA, 87 mujeres caucásicas y 217 hombres caucásicos (fig. 1). La presión arterial (PA) fue mayor en hombres de OA (152 ± 19/93 ± 14 mmHg) seguido de mujeres de OA (148 ± 19/91 ± 11 mmHg), hombres caucásicos (145 ± 16/88 ± 1 mmHg) y mujeres caucásicas (142 ± 17/90 ± 90 mmHg), p < 0,01. La VOP fue mayor en mujeres de OA (10,4 ± 2,5 m/s), seguido de hombres de OA (10,1 ± 2,3 m/s), mujeres caucásicas (9,9 ± 2,1 m/s) y hombres caucásicos (9,4 ± 2,2 m/s), p < 0,01. La prevalencia de daño renal fue mayor en hombres y mujeres de OA (34,2% y 27,6%, respectivamente) comparado con hombres y mujeres caucásicas (14,3% y 10,3%, respectivamente), p < 0,01 (tabla 1). Los análisis multivariados ajustados por edad, IMC, PA, frecuencia cardíaca, diabetes, dislipemia, tratamiento farmacológico para HTA, tabaco, cociente aldosterona/renina y función renal, mostraron que las personas de OA tenían más daño renal, con (odds ratio (OR), 95% intervalo de confianza (IC)) 3,5(1,3; 9,5) en mujeres y 4,3(1,7; 11,0) en hombres, p < 0,05; comparado con mujeres caucásicas (tabla 2). Otros factores asociados a daño renal tras ajustar por múltiples confusores fueron edad, PA, y tratamiento para la HTA. Por otro lado, la VOP fue mayor en mujeres (β = 0,7 m/s, p = 0,030 en caucásicas, β = 0,5 m/s, p = 0,046 en OA), comparado con hombres caucásicos (tabla 2, fig. 2). Otros factores asociados a cambios en la VOP tras ajustar por múltiples confusores fueron edad, diabetes, PA, FC y función renal.
|
Tabla 1 |
||||||
|
|
Total (N = 654) |
Mujeres caucásicas (N = 87) |
Hombres caucásicos (N = 217) |
Mujeres de OA (N = 163) |
Hombres de OA (N = 187) |
p |
|
n (%) |
n (%) |
n (%) |
n (%) |
n (%) |
||
|
Edad (años), media (DE) |
44 (14) |
43 (15) |
44 (15) |
45 (13) |
44 (12) |
0,6005 |
|
Hipertensión arterial |
||||||
|
Duración HTA (meses), media (DE), N = 558 |
71,5 (84,4) |
52,4 (67,7) |
64,0 (74,4) |
86,0 (105,2) |
76,0 (79,5) |
0,0195 |
|
Tratamiento para HTA, N = 651 |
470 (71,9) |
51 (58,6) |
137 (63,1) |
130 (79,8) |
152 (81,3) |
< 0,0001 |
|
Presión arterial sistólica (mmHg), media (DE), N = 635 |
147,3 (18,4) |
141,6 (17,0) |
145,5 (16,3) |
147,8 (19,4) |
151,7 (19,6) |
0,0001 |
|
Presión arterial diastólica (mmHg), media (DE), N = 635 |
90,6 (12,5) |
90,3 (13,5) |
88,3 (11,3) |
90,9 (11,2) |
93,1 (14,0) |
0,0023 |
|
Frecuencia cardíaca (latidos por minuto), media (DE), N = 622 |
71,4 (14,4) |
74,4 (15,0) |
69,4 (13,7) |
71,5 (10,9) |
92,1 (17,1) |
0,0460 |
|
Renina (mU/L), media (DE), N = 610 |
54,77 (282,68) |
46,29 (70,83) |
111,60 (481,84) |
14,86 (27,86) |
27,97 (51,25) |
0,0048 |
|
Aldosterona (pmol/L), media (DE), N = 617 |
448,56 (335,50) |
404,28 (225,22) |
395,79612 (306,73) |
490,88 (304,43) |
493,15 (416,31) |
0,0069 |
|
Cociente aldosterona-renina, media (DE), N = 607 |
92,47 (216,56) |
43,20 (76,47) |
37,76 (104,37) |
183,92 (315,22) |
99,07 (225,16) |
< 0,0001 |
|
Perfil de riesgo cardiovascular |
||||||
|
Dislipidemia, N = 603 |
325 (49,7) |
41 (47,1) |
122 (56,2) |
74 (45,4) |
88 (47,1) |
0,251 |
|
TG (mg/dL), media (DE), N = 585 |
122,12 (85,84) |
130,09 (76,99) |
148,67 (107,96) |
94,69 (53,1) |
110,62 (73,45) |
< 0,0001 |
|
CT (mg/dL), media (DE), N = 590 |
186,87 (45,56) |
198,46 (42,47) |
190,73 (42,86) |
186,87 (54,83) |
177,61 (37,45) |
0,0043 |
|
HDL (mg/dL), media (DE), N = 586 |
56,06 (17,79) |
64,96 (18,17) |
53,36 (18,17) |
59,93 (17,40) |
51,81 (14,31) |
< 0,0001 |
|
LDL (mg/dL), media (DE), N = 584 |
106,71 (35,96) |
108,26 (35,96) |
109,04 (39,44) |
105,56 (31,32) |
104,40 (34,80) |
0,6271 |
|
Diabetes, N = 653 |
88 (13,46) |
9 (10,34) |
19 (8,76) |
30 (18,40) |
30 (16,04) |
0,081 |
|
HbA1c (%), media (DE), N = 528 |
5,8 (3,2) |
5,7 (2,8) |
5,6 (3,1) |
6,0 (3,3) |
6,0 (3,2) |
0,0016 |
|
IMC (Kg/m2), media (DE), N = 608 |
29,68 (5,50) |
28,85 (6,58) |
28,89 (5,22) |
30,47 (5,93) |
30,27 (4,61) |
0,0106 |
|
Tabaco (actual), N = 608 |
78 (11,93) |
15 (17,24) |
39 (17,97) |
7 (4,29) |
17 (9,09) |
< 0,0001 |
|
Evento cardiovascular, N = 635 |
27 (4,13) |
1 (1,15) |
10 (4,61) |
6 (3,68) |
10 (5,35) |
0,383 |
|
Daño vascular y renal |
||||||
|
VOP (m/s), media (DE), N = 539 |
9,93 (2,33) |
9,88 (2,09) |
9,42 (2,20) |
10,40 (2,51) |
10,15 (2,34) |
0,0014 |
|
Creatinina (mg/dl), media (DE), N = 647 |
1,01 (0,35) |
0,75 (0,12) |
1,0 (0,22) |
0,89 (0,35) |
1,23 (0,41) |
< 0,0001 |
|
eGFR (ml/min), N = 647 |
88,53 (21,38) |
100,80 (17,06) |
92,42 (17,96) |
87,94 (23,50) |
78,87 (20,83) |
< 0,0001 |
|
Cociente albúmina-creatinina (orina), N = 460 |
||||||
|
> 300 mg/g |
21 (3,21) |
0 (0,00) |
7 (3,23) |
6 (3,68) |
8 (4,28) |
0,035 |
|
30-300 mg/g |
86 (13,15) |
9 (10,34) |
21 (9,68) |
24 (14,72) |
32 (17,11) |
|
|
< 30 mg/g |
353 (53,98) |
44 (50,57) |
136 (62,67) |
83 (50,92) |
90 (48,13) |
|
|
Daño renal, N = 580 |
149 (22,78) |
9 (10,34) |
31 (14,29) |
45 (27,61) |
64 (34,22) |
< 0,0001 |
|
Tabla 2 |
|||||
|
Variables de regresión logística |
OR (IC95%) |
p |
Variables de regresión lineal |
Coeficiente-β (DE) |
p |
|
Intersección de sexo y etnia * |
Intersección de sexo y etnia ** |
||||
|
Hombres caucásicos |
1,24 (0,47; 3,26) |
0,659 |
Mujeres caucásicas |
0,67 (0,06; 1,27) |
0,030 |
|
Mujeres de OA |
3,54 (1,33; 9,46) |
0,012 |
Mujeres de OA |
0,53 (0,01; 1,05) |
0,046 |
|
Hombres de OA |
4,28 (1,66; 11,04) |
0,003 |
Hombres de OA |
0,21 (-0,28; 0,71) |
0,397 |
|
Edad |
1,04 (1,02; 1,06) |
< 0,001 |
Edad |
0,09 (0,72; 0,10) |
< 0,001 |
|
Tabaco |
1,33 (0,61; 2,89) |
0,477 |
Tabaco |
0,38 (-0,19; 0,95) |
0,190 |
|
Diabetes |
1,34 (0,67; 2,68) |
0,404 |
Diabetes |
1,00 (0,44; 1,56) |
< 0,001 |
|
Dislipidemia |
1,05 (0,64; 1,73) |
0,851 |
Dislipidemia |
0,03 (-0,35; 0,41) |
0,883 |
|
IMC |
1,05 (1,01; 1,10) |
0,038 |
IMC |
0,02 (-0,02; 0,57) |
0,251 |
|
Tensión arterial sistólica |
1,02 (1,00; 1,04) |
0,001 |
Tensión arterial diastólica |
0,03 (0,01; 0,04) |
< 0,001 |
|
Frecuencia cardíaca |
1,00 (0,98; 1,02) |
0,992 |
Frecuencia cardíaca |
0,02 (0,01; 0,04) |
< 0,001 |
|
Tratamiento de la HTA |
2,44 (1,21; 4,92) |
0,013 |
Tratamiento de la HTA |
-0,10 (-0,52; 0,32) |
0,641 |
|
Cociente aldosterona/renina |
1,00 (0,99; 1,01) |
0,074 |
Cociente aldosterona/renina |
0,01 (-0,01; 0,01) |
0,158 |
|
- |
- |
- |
Creatinina |
0,01 (0,01; 0,02) |
0,006 |
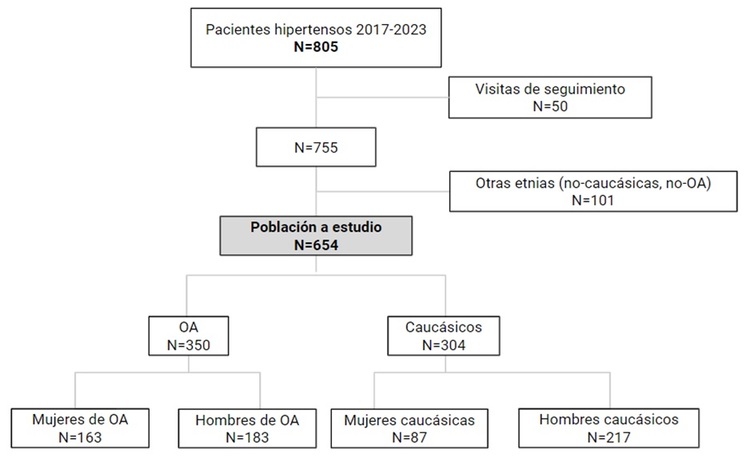
Figura 1.
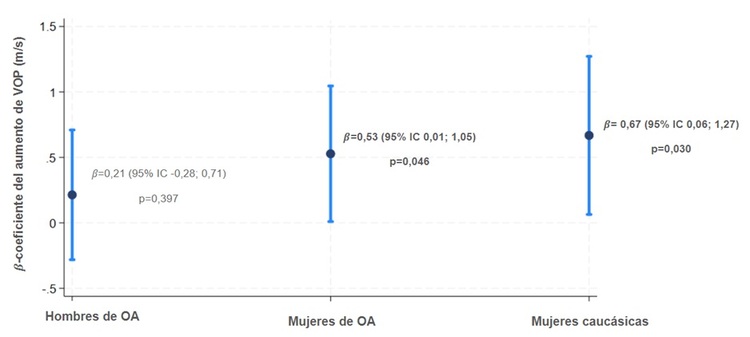
Figura 2.
Conclusiones: Los hombres de OA hipertensos tienen mayor riesgo de daño renal, seguidos por las mujeres de OA. Las mujeres caucásicas hipertensas tienen mayor rigidez arterial, seguidas por las mujeres de OA. El estudio de la intersección entre determinantes de salud como la etnia y sexo, permite entender desigualdades entre subgrupos y poder dirigir y personalizar intervenciones.






