Desde su aparición en diciembre de 2019, la enfermedad por coronavirus causada por el síndrome respiratorio agudo severo coronavirus2 se ha convertido en una emergencia mundial, propagándose rápidamente por todo el mundo. En respuesta a la derivación temprana de estos pacientes a centros de salud ambulatorios, decidimos buscar tratamientos más eficaces en las primeras etapas de su derivación. Este estudio tiene como objetivo prevenir tanto la progresión como el deterioro de las condiciones físicas de los pacientes con COVID-19, reducir la tasa de derivaciones y mitigar los riesgos de hospitalización y de muerte.
Material y métodosRealizado en el Centro Terapéutico Dibaj, ciudad de Hamadan, Irán, un ensayo controlado aleatorizado doble ciego abarcó 225 pacientes con COVID-19 de abril a septiembre de 2022. Se obtuvo la aprobación ética de la Universidad de Ciencias Médicas de Hamadan (Aprobación n.° IR.UMSHA .REC.1400.957), con el protocolo registrado en el Registro Iraní de Ensayos Clínicos (Registro n.° IRCT20220302054167N1). Los pacientes cumplieron con el diagnóstico de COVID-19 a través de la presentación de síntomas y la confirmación por PCR, excluyendo aquellos con antecedentes de vacunas y afectación de órganos. Los pacientes con una saturación de oxígeno superior al 92% se asignaron a tres grupos: el grupoA recibió N-acetilcisteína, el grupoB recibió bromhexina y el grupoC recibió atención estándar. Los seguimientos de los niveles de oxígeno, los síntomas y las necesidades de hospitalización se realizaron los días7 y 14, con pacientes hospitalizados monitorizados durante un mes después de la hospitalización.
ResultadosEl estudio encontró que tanto la N-acetilcisteína como la bromhexina pueden reducir efectivamente las tasas de hospitalización y la mortalidad y acortar la duración de la hospitalización. La tercera visita de los pacientes que recibieron N-acetilcisteína mostró un aumento del 1,33% en la saturación de oxígeno en comparación con su primera visita, y en los pacientes que recibieron bromhexina este aumento fue del 1,19%. La tasa de mortalidad fue del 9,33% en el grupo control y nula en ambos grupos de pacientes que recibieron medicación.
ConclusiónLos resultados de este estudio indican que la N-acetilcisteína y la bromhexina pueden ser efectivas en el tratamiento de pacientes con COVID-19 positivo, con una tasa de hospitalización más baja, una hospitalización más corta, un tiempo de recuperación más rápido y una mortalidad reducida en comparación con el grupo control.
Since its emergence in December 2019, the coronavirus disease caused by the severe acute respiratory syndrome coronavirus2 has become a global emergency, spreading rapidly worldwide. In response to the early referral of these patients to outpatient health centers, we decided to seek more effective treatments in the early stages of their referral. This study aims to prevent both the progression and deterioration of the physical conditions of COVID-19 patients, reduce the rate of referrals, and mitigate the risks of hospitalization and death.
Material and methodsConducted at Dibaj Therapeutic Center, Hamadan City, Iran, a double-blind randomized controlled trial encompassed 225 COVID-19 patients from April to September 2022. Ethical approval was obtained from Hamadan University of Medical Sciences (Approval No.: IR.UMSHA.REC.1400.957), with the protocol registered in the Iranian Registry of Clinical Trials (Registration No.: IRCT20220302054167N1). In this study, we included patients who tested positive for COVID-19 PCR and were symptomatic, excluding those who were pregnant or had received a COVID-19 vaccine. Patients with oxygen saturation above 92% were allocated to three groups: GroupA received N-acetylcysteine, GroupB received Bromhexine, and GroupC received standard care. Follow-ups on oxygen levels, symptoms, and hospitalization needs were conducted on days 7 and 14, with hospitalized patients monitored for one month post-hospitalization.
ResultsThe study found that both N-acetylcysteine and Bromhexine can effectively reduce hospitalization rates and mortality and shorten the duration of hospitalization. The third visit of patients who received N-acetylcysteine showed an increase of 1.33% in oxygen saturation compared to their first visit, and in patients who received Bromhexine, this increase was 1.19%. The mortality rate was 9.33% in the control group and zero in both groups of patients who received medication.
ConclusionIn conclusion, the results of this study indicate that N-acetylcysteine and bromhexine may be effective in the treatment of patients with positive COVID-19, with a lower hospitalization rate, shorter hospitalization, faster recovery time, and reduced mortality compared to the control group.
Desde su aparición en diciembre de 2019, la enfermedad por coronavirus (COVID-19) causada por el coronavirus2 (SARS-CoV-2) del síndrome respiratorio agudo severo se ha convertido en una emergencia a nivel mundial, extendiéndose rápidamente por todo el mundo1. Aunque la COVID-19 puede presentarse con síntomas leves, como fiebre, tos y pérdida del olfato o del gusto, también puede dar lugar a casos graves con afectación pulmonar extensa, síndrome de dificultad respiratoria aguda, hospitalización, intubación e incluso la muerte2. Esta situación disminuye el contenido de oxígeno en la sangre del paciente. La producción de citocinas y de quimiocinas es una de las principales respuestas inmunitarias durante la infección vírica3. Se han notificado grandes cantidades de IL-8, un potente factor quimiotáctico para los neutrófilos, en pacientes con SARS4,5. En los pacientes de COVID-19 graves, el aumento del número de neutrófilos está asociado a la gravedad de la enfermedad6. La producción de altos niveles de citocinas proinflamatorias da lugar a una «tormenta de citocinas»2,7. Cuando el paciente es ingresado en el hospital, lo más probable es que la enfermedad ya haya alcanzado la segunda o tercera fase, con problemas respiratorios y fallo multiorgánico. Por lo tanto, a partir del segundo paso, debemos mirar más allá del virus y centrarnos en la tormenta de citoquinas y de radicales libres como agentes patógenos8.
La N-acetilcisteína (NAC) se emplea desde hace tiempo para tratar la intoxicación causada por el paracetamol (acetaminofeno)9 y como mucolítico en las enfermedades pulmonares crónicas. La NAC también es un antioxidante y puede reducir el estrés oxidativo7 como profármaco, ya que se transforma en L-cisteína10, que es el precursor del antioxidante biológico glutatión. Por este motivo, la administración de NAC renueva las fuentes de glutatión. La NAC también muestra algunos efectos antiinflamatorios a través de la inhibición de NF-κB mediante la activación de la regeneración del factor nuclear kappa cinasa modulando, de este modo, la síntesis de citocinas. La replicación de los virus que contienen ARN requiere el apoyo de una vía NF-κB activa en las células huésped. En cuanto a los coronavirus humanos (HCoV-229E), la supresión de NF-κB reduce significativamente la tasa de replicación. De este modo, los fármacos capaces de inhibir la activación de NF-κB pueden disminuir la replicación del virus2,11. Además, la NAC ha presentado mecanismos protectores frente a diversas afecciones asociadas a la COVID-19, como, por ejemplo, las enfermedades cardiovasculares12. En cuanto a la lesión cardiaca y la trombosis como complicaciones potencialmente mortales de la COVID-19, la NAC por vía intravenosa ha mostrado los efectos vasodilatadores, antiinflamatorios y antiagregantes de la nitroglicerina que pueden ser beneficiosos para la mejora de los resultados, como el infarto agudo de miocardio, la angina inestable y el edema agudo de pulmón13. En algunos estudios el fármaco NAC también se ha recomendado como agente protector durante la reperfusión, ayudando a prevenir el daño tisular endotelial14. Las complicaciones cardiovasculares son manifestaciones frecuentes tanto de las secuelas agudas como postagudas de la infección por COVID-19. Estas abarcan diversos trastornos cardiovasculares, como lesiones miocárdicas, síndromes coronarios agudos, miocarditis, miocardiopatías, arritmias, insuficiencia cardiaca y trombosis venosa profunda15.
La bromhexina actúa descomponiendo y diluyendo las secreciones mucosas de las vías respiratorias, lo que facilita su expulsión. Esto ayuda a aliviar síntomas como la tos, la congestión y la dificultad para respirar. Además, se ha demostrado que la bromhexina tiene efectos antiinflamatorios, lo que puede ayudar a reducir la hinchazón y la irritación de las vías respiratorias16. La bromhexina cuenta con una larga historia de uso en trastornos de las vías respiratorias y ha sido ampliamente estudiada por su eficacia en el tratamiento de estas afecciones. En general, se tolera bien y se han descrito pocos efectos secundarios. En conjunto, la bromhexina es una herramienta importante en el tratamiento de los trastornos de las vías respiratorias caracterizados por secreciones mucosas espesas y pegajosas. Su eficacia como expectorante y mucolítico la convierte en una valiosa opción para quienes buscan alivio de los síntomas respiratorios17.
En medio de la actual pandemia de COVID-19, es de suma importancia prevenir la hospitalización y mejorar la recuperación de los pacientes ambulatorios. Para abordar esta cuestión, se ha llevado a cabo un ensayo clínico aleatorizado en el que se ha comparado la eficacia de la NAC con la de la bromhexina. Nuestro objetivo era encontrar opciones de tratamiento eficaces que pudieran ayudar a controlar los síntomas de la COVID-19, así como prevenir la progresión de la enfermedad y las complicaciones, reduciendo potencialmente la carga sobre los sistemas hospitalarios y la mortalidad por COVID-19.
MétodosDiseño y ámbito del estudioSe llevó a cabo un ensayo doble ciego, aleatorizado y controlado en 225 pacientes ambulatorios que había sufrido COVID-19 tratados en el Centro Terapéutico Dibaj, de la ciudad de Hamadán, Irán. Todo el proceso del estudio fue aprobado por el Comité de Ética de Investigación de la Universidad de Ciencias Médicas de Hamadán (n.° IR.UMSHA.REC.1400.957), y el protocolo fue registrado en el Registro Iraní de Ensayos Clínicos (n.° IRCT20220302054167N1) entre los meses de abril y septiembre de 2022. El diagnóstico de COVID-19 se basó en los síntomas que presentaban los pacientes, que incluían tos, fiebre, debilidad, letargo, dolores musculares, secreción nasal y dolor de garganta. Se recogieron muestras nasales y/o faríngeas de los pacientes para realizar una prueba de reacción en cadena de la polimerasa con transcriptasa inversa (RT-PCR, por sus siglas en inglés) con el fin de confirmar el diagnóstico de COVID-19 en el centro de servicios sanitarios, y solo se incluyó en el estudio a los pacientes con resultados positivos en la PCR. Cabe destacar que se incluía a los pacientes en el estudio solo si no era necesaria su derivación y no había evidencias de afectación orgánica, incluidos los pulmones, tras una tomografía computarizada (TAC) torácica realizada en la visita inicial, y nunca habían recibido vacunación para la COVID-19. En un primer momento, se determinó la saturación de O2 (SpO2) del paciente con un oxímetro de pulso y, si esta era superior al 92%, este era incluido en el estudio; de este modo, 225 participantes fueron asignados aleatoriamente a tres grupos (A, B y C). El grupoA recibió 600mg de NAC por vía oral dos veces al día durante cinco días, mientras que el grupoB recibió comprimidos de 8mg de bromhexina tres veces al día durante cinco días. El tercer grupo de control (grupoC) recibió únicamente los tratamientos rutinarios y habituales prescritos para los otros dos grupos. Todos los pacientes tomaron 250mg de naproxeno dos veces al día durante cinco días, 20mg de famotidina una vez al día durante diez días, 50.000 unidades de vitaminaD a la semana durante cuatro semanas y 1.000mg de vitaminaC diarios. A continuación, se pidió a los pacientes que volvieran al centro a los 7 y 14 días para comprobar sus niveles de oxígeno, controlar los cambios en sus síntomas, someterse a los exámenes necesarios y ser informados de si era necesaria su hospitalización. Todos los pacientes ingresados en el hospital fueron objeto de seguimiento durante un mes tras la hospitalización, controlando la duración de su estancia, su estado general y la tasa de mortalidad. Los resultados de los exámenes y las características de los pacientes también se registraron en una lista de control diseñada a tal efecto.
Objetivos e hipótesisEl objetivo primario del plan es comparar los efectos de dos fármacos, acetilcisteína y bromhexina, sobre la tasa de recuperación y prevención de la hospitalización en pacientes ambulatorios y la tasa de mortalidad, con los pacientes del grupo de control. El estudio tiene como objetivo investigar exhaustivamente diversos aspectos relativos a los pacientes con COVID-19 que acuden al Centro Dibaj. Estos incluyen determinar la frecuencia de COVID-19 entre los pacientes ambulatorios en función de la información demográfica, evaluar la variabilidad de los niveles de oxígeno durante las visitas al centro y explorar la prevalencia de los síntomas en el momento de las visitas. Además, la investigación consiste en comparar el porcentaje medio de saturación de oxígeno antes y después del uso de NAC y bromhexina, ambos en los días 7 y 14 de la enfermedad. Así mismo, se estudia la frecuencia y la duración de la hospitalización entre los pacientes tratados con NAC y bromhexina, así como entre los pacientes del grupo de control. Las hipótesis asociadas a estos objetivos abordan las variaciones en la incidencia, los niveles de oxígeno, la prevalencia de síntomas y los patrones de hospitalización en los distintos grupos y modalidades de tratamiento.
Método de muestreoSe empleó un método de aleatorización en seis bloques para la asignación de los pacientes. Se prepararon hojas de papel con las letras A, B y C escritas en dos hojas cada una. Estas hojas se barajaron y se colocaron en un cajón del escritorio. En el momento de la elegibilidad del paciente, se extrajo aleatoriamente una hoja y se asignó al paciente al grupo A, B, C o ningún fármaco. Es importante señalar que una hoja en concreto no se devolvía al cajón hasta que no se habían extraído las seis hojas al menos una vez. Este proceso de asignación aleatoria se volvía a repetir para los seis pacientes siguientes hasta alcanzar el tamaño de muestra deseado de 225 pacientes.
Método enmascaradoLos tres grupos de intervención y control recibieron medicamentos con el mismo aspecto, identificados con el mismo código. Ni los pacientes ni los examinadores conocían el tipo concreto de medicación prescrita. Por ello, el estudio se realizó según un régimen doble ciego.
Criterios de inclusiónSe incluyeron pacientes adultos de entre 18 y 80años con síntomas indicativos de COVID-19 que acudieron al Centro Dibaj durante los tres días siguientes al inicio de los síntomas y tenían un resultado positivo en la prueba de RT-PCR, una SpO2>92% y una TAC torácica normal en su visita inicial. Se incluyó en esta investigación a pacientes sin dificultad respiratoria y que no habían recibido ninguna vacunación para la COVID-19.
Criterios de exclusiónNo se incluyó a los pacientes que no cumplían los siguientes criterios: aquellos sometidos a otros tratamientos, pacientes con IMC<18,5 e IMC>25, pacientes con situaciones subyacentes como embarazadas o lactantes, pacientes que estaban recibiendo nitroglicerina, aquellos que mostraban indicios de afectación pulmonar (niveles de oxígeno >92%, síntomas persistentes de disnea y dolor torácico, y evidencia de afectación pulmonar observada en la TAC) que requerían hospitalización o remisión a un hospital, según la recomendación del especialista en enfermedades infecciosas del hospital, y aquellos que tenían antecedentes de alergia o de choque anafiláctico debido a la NAC o la bromhexina o que habían experimentado efectos secundarios durante su uso.
Método de análisis de los datosSe utilizó la prueba de la t independiente para comparar variables cuantitativas, la prueba de la chi-cuadrado para comparar variables cualitativas y la prueba ANOVA para comparar las medias de tres o más grupos. En caso necesario, los resultados se analizaron mediante un modelo de regresión de Poisson. Todos los análisis estadísticos se realizaron con un nivel de confianza del 95% utilizando el programa Stata, versión 16.
ResultadosEl presente estudio tenía como objetivo investigar la eficacia de la NAC y la bromhexina en el tratamiento de pacientes positivos para COVID-19. En el estudio se incluyeron un total de 225 pacientes ambulatorios que fueron remitidos al Centro Médico Dibaj tras dar positivo en la prueba de PCR para la COVID-19. Los pacientes se asignaron aleatoriamente a uno de entre tres grupos: 75 pacientes recibieron NAC, 75 pacientes fueron tratados con bromhexina y 75 pacientes sirvieron como grupo de control y no recibieron medicación. Entre la muestra total, 110 individuos (48,9%) eran mujeres y 115 individuos (51,1%) eran hombres. La media de edad de los pacientes era de 45,31±14,884 años, con un intervalo entre 18 y 80años. De los 225 pacientes, 152 (67,6%) no padecían ninguna enfermedad subyacente, 29 (12,9%) tenían hipertensión, 21 (9,3%) sufrían enfermedades cardiovasculares, 15 (6,7%) tenían diabetes y 4 individuos (1,8%) padecían cáncer. Además, 4 individuos (1,8%) padecían otras enfermedades.
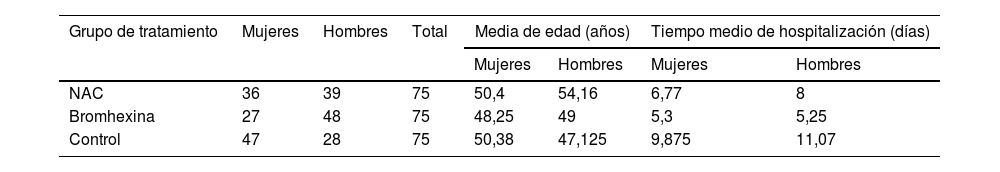
De los 225 pacientes, 38 (16,88%) habían estado hospitalizados, mientras que 187 (83,11%) no presentaban antecedentes de hospitalización en el plazo de un mes. En el grupo NAC, 11 de los 75 pacientes (14,66%) fueron ingresados en el hospital, mientras que los 64 pacientes restantes (85,33%) se recuperaron en casa sin hospitalización. En el grupo de bromhexina, 6 de los 75 pacientes (8%) fueron hospitalizados, y los 69 pacientes restantes (92%) fueron tratados en casa sin necesidad de hospitalización. En el grupo de control, 21 de los 75 pacientes (28%) ingresaron en el hospital, y los 54 restantes (72%) fueron tratados en casa sin hospitalización. En general, la media de edad de los pacientes hospitalizados era de 55,15años, oscilando entre 24 y 80años. De los 38 pacientes ingresados en el hospital, el 58,8% tenían más de 60años, mientras que el 45,31% eran menores de 60años (tabla 1).
Comparación de los resultados del tratamiento de los pacientes con COVID-19: análisis basado en el sexo
| Grupo de tratamiento | Mujeres | Hombres | Total | Media de edad (años) | Tiempo medio de hospitalización (días) | ||
|---|---|---|---|---|---|---|---|
| Mujeres | Hombres | Mujeres | Hombres | ||||
| NAC | 36 | 39 | 75 | 50,4 | 54,16 | 6,77 | 8 |
| Bromhexina | 27 | 48 | 75 | 48,25 | 49 | 5,3 | 5,25 |
| Control | 47 | 28 | 75 | 50,38 | 47,125 | 9,875 | 11,07 |
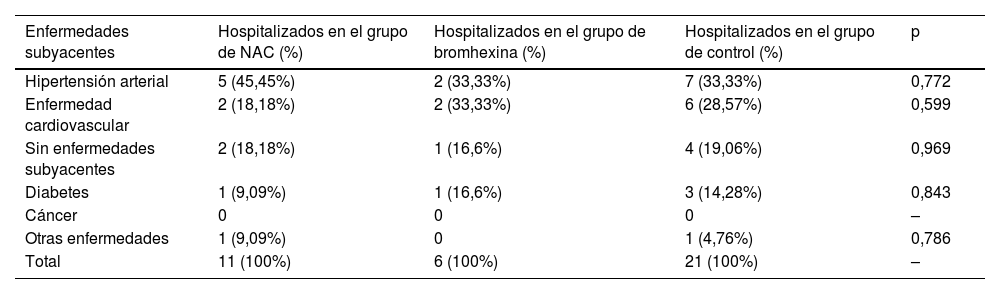
La asociación entre las tasas de hospitalización y las enfermedades subyacentes de los pacientes es la siguiente: de los 38 pacientes hospitalizados, 14 (36,82%) tenían hipertensión, 10 (26,31%) padecían enfermedad cardiovascular, 7 (18,42%) no presentaban enfermedades subyacentes, 5 (13,15%) tenían diabetes y 2 (5,26%) padecían otras enfermedades. Además, la comparación de las tasas de hospitalización por diferentes enfermedades subyacentes entre los grupos de NAC, bromhexina y control no mostró diferencias estadísticamente significativas (p>0,05) (tabla 2).
Comparación de las tasas de hospitalización por diferentes enfermedades subyacentes entre los grupos de NAC, bromhexina y control: Análisis mediante chi cuadrado
| Enfermedades subyacentes | Hospitalizados en el grupo de NAC (%) | Hospitalizados en el grupo de bromhexina (%) | Hospitalizados en el grupo de control (%) | p |
|---|---|---|---|---|
| Hipertensión arterial | 5 (45,45%) | 2 (33,33%) | 7 (33,33%) | 0,772 |
| Enfermedad cardiovascular | 2 (18,18%) | 2 (33,33%) | 6 (28,57%) | 0,599 |
| Sin enfermedades subyacentes | 2 (18,18%) | 1 (16,6%) | 4 (19,06%) | 0,969 |
| Diabetes | 1 (9,09%) | 1 (16,6%) | 3 (14,28%) | 0,843 |
| Cáncer | 0 | 0 | 0 | – |
| Otras enfermedades | 1 (9,09%) | 0 | 1 (4,76%) | 0,786 |
| Total | 11 (100%) | 6 (100%) | 21 (100%) | – |
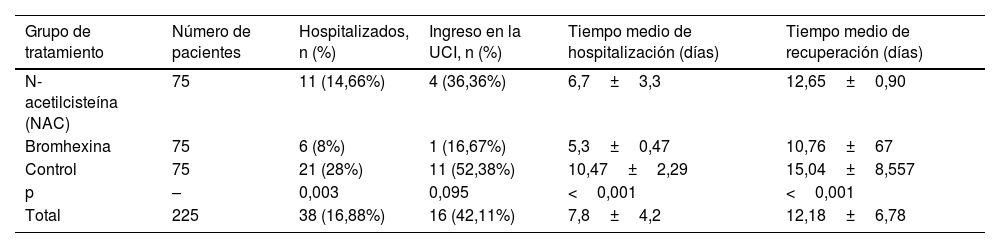
En el grupo de NAC, 4 (4,4%) de los 11 pacientes hospitalizados requirieron ingreso en la UCI, mientras que solo uno (2,4%) de los 6 pacientes hospitalizados en el grupo de bromhexina lo requirió. En el grupo de control, 11 (10,2%) de los 21 pacientes hospitalizados requirieron ingreso en la UCI. El tiempo medio de hospitalización fue de 5,8, de 5 y de 9,63 días para los grupos A, B y C, respectivamente. En el grupo de la bromhexina, el tiempo medio de hospitalización fue de 5,25días en los hombres y de 5,3días en las mujeres. En el grupo de NAC, el tiempo medio de hospitalización fue de 5,4días en las mujeres y de 8días en los hombres. En el grupo de control, el tiempo medio de hospitalización fue de 11,07días en los hombres y de 9,875días en las mujeres, respectivamente, y la diferencia entre estos tres grupos era estadísticamente significativa (p=0,766). En general, el tiempo medio de recuperación de los pacientes (desviación estándar) desde la aparición de los síntomas hasta el final de los mismos fue de 12,18 (6,78) días, con unos periodos de recuperación mínimo y máximo respectivos de 3 y 40días tras la aparición de los síntomas. La duración media de la recuperación completa de los síntomas en los grupos de NAC y bromhexina fue de 12,65±0,90 y de 10,76±0,64 (p=0,0935), respectivamente, sin mostrar diferencias estadísticamente significativas, aunque en el grupo control fue de 15,04±8,557 (p=0,0001), mostrando diferencias estadísticamente significativas (tabla 3).
Resultados de los tres grupos de tratamiento (N-acetilcisteína, bromhexina, control) de este estudio
| Grupo de tratamiento | Número de pacientes | Hospitalizados, n (%) | Ingreso en la UCI, n (%) | Tiempo medio de hospitalización (días) | Tiempo medio de recuperación (días) |
|---|---|---|---|---|---|
| N-acetilcisteína (NAC) | 75 | 11 (14,66%) | 4 (36,36%) | 6,7±3,3 | 12,65±0,90 |
| Bromhexina | 75 | 6 (8%) | 1 (16,67%) | 5,3±0,47 | 10,76±67 |
| Control | 75 | 21 (28%) | 11 (52,38%) | 10,47±2,29 | 15,04±8,557 |
| p | – | 0,003 | 0,095 | <0,001 | <0,001 |
| Total | 225 | 38 (16,88%) | 16 (42,11%) | 7,8±4,2 | 12,18±6,78 |
Los datos incluyen los porcentajes de hospitalización e ingreso en la UCI, así como los tiempos medios de hospitalización y recuperación. Los análisis estadísticos incluyen la prueba de chi-cuadrado para los porcentajes de hospitalización e ingreso en la UCI, y ANOVA unidireccional para los tiempos medios de hospitalización y recuperación, seguido de pruebas post hoc para diferencias significativas
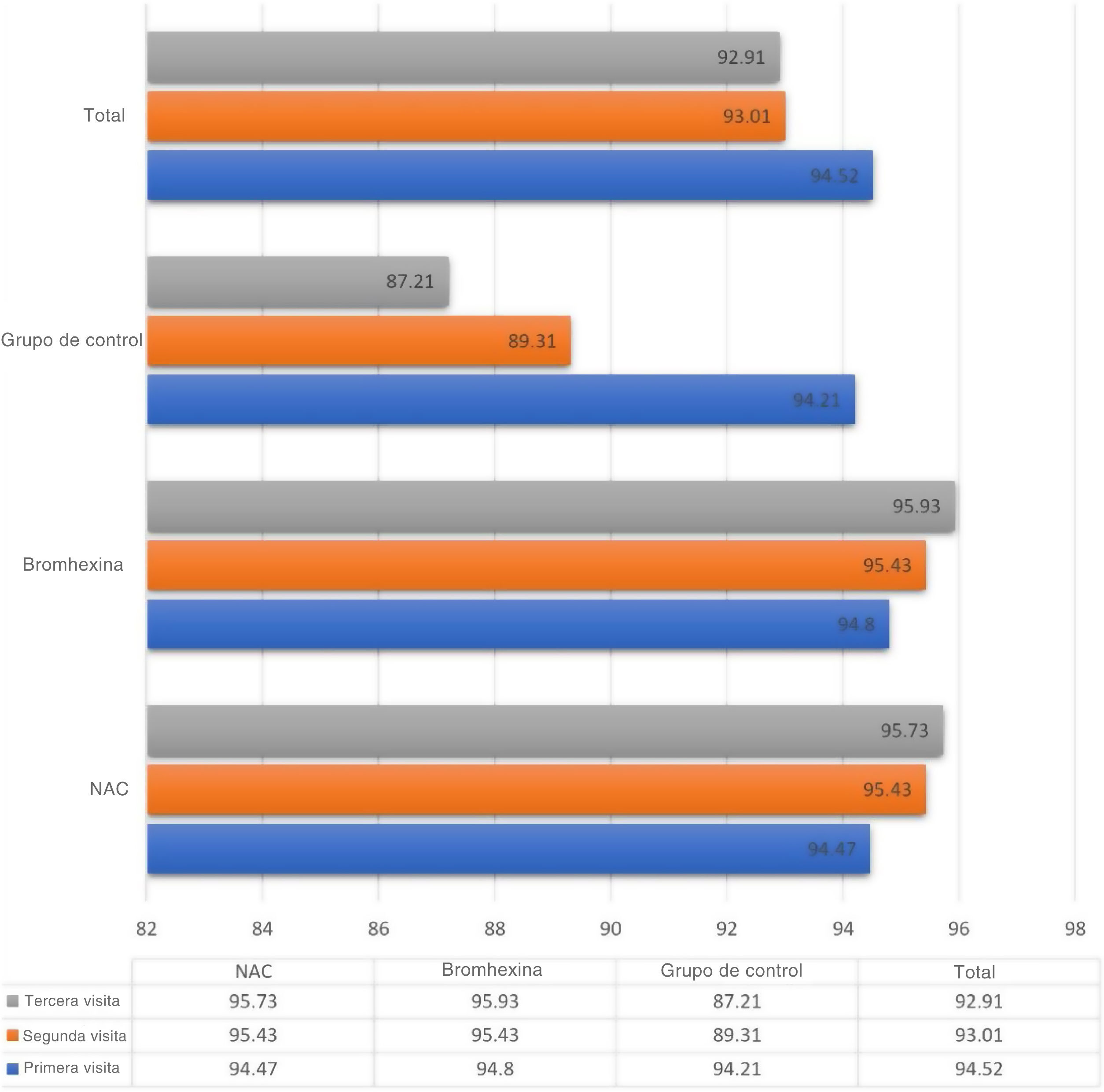
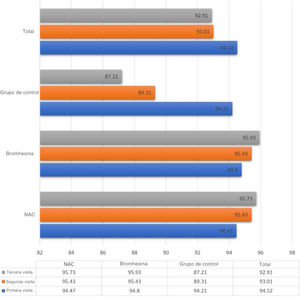
Los niveles medios de saturación de oxígeno en los tres grupos de estudio mostraron variaciones matizadas. En la visita inicial, todos los grupos manifestaban una saturación media comparable del 94,52±2,502%. Las evaluaciones posteriores en los días séptimo y decimocuarto mostraron un descenso al 93,01±6,862% y al 92,91±12,55%, respectivamente.
Tras un examen más detallado dentro del grupo de NAC, la saturación de oxígeno mostró tendencias características en las visitas secuenciales: 94.47%, 95,43% y 95,73% en la primera, segunda y tercera visita, respectivamente. De forma análoga, el grupo de bromhexina mostró niveles del 94,80%, del 95,43% y del 95,93% durante las visitas correspondientes. Por el contrario, en el grupo de control sin tratamiento la saturación de oxígeno descendió del 94,21% al 89,31%, y posteriormente hasta el 87,21% durante la primera, la segunda y la tercera visita, respectivamente.
La aplicación de la prueba ANOVA arrojó resultados significativos en los niveles de saturación de oxígeno:
- •
El primer día no se observaron divergencias estadísticamente significativas en la concentración media de oxígeno de los tres grupos (p=0,393).
- •
Al séptimo día se observaba una diferencia significativa (p<0,001), con los grupos de NAC y bromhexina mostrando concentraciones notablemente superiores en comparación con el grupo de control.
- •
Se observó un patrón similar al decimocuarto día, lo que significaba una disparidad significativa (p<0,001) en la concentración de oxígeno, favorable para los grupos de NAC y bromhexina.
Un examen más detenido de los niveles de saturación de oxígeno permitió aclarar una dinámica temporal convincente:
- •
Entre la primera y la segunda visita los grupos de NAC y bromhexina mostraron un aumento estadísticamente significativo, mientras que el grupo de control experimentó un descenso (p<0,001).
- •
De forma análoga, entre la segunda y la tercera visita los grupos de NAC y bromhexina mostraron un aumento de los niveles de saturación, mientras que en el grupo de control se observó un descenso (p<0,001) (fig. 1).
En particular, las tasas de mortalidad fueron nulas en los gruposA (NAC) yB (bromhexina), en contraste con las siete muertes (9,33%) registradas en el grupoC (control). Cabe destacar que el 78% de los pacientes no notificaron complicaciones tras la medicación, mientras que 33 individuos notificaron complicaciones leves, en su mayoría gestionables sin intervención. El análisis en profundidad dentro de los grupos de NAC y bromhexina mostró complicaciones específicas, que incluían reducción de la presión arterial y dolor de estómago en el grupo de NAC, y somnolencia en el de bromhexina, sin que se informara de interrupciones del tratamiento del estudio debido a complicaciones. Cabe destacar que ningún paciente se retiró del estudio debido a efectos adversos.
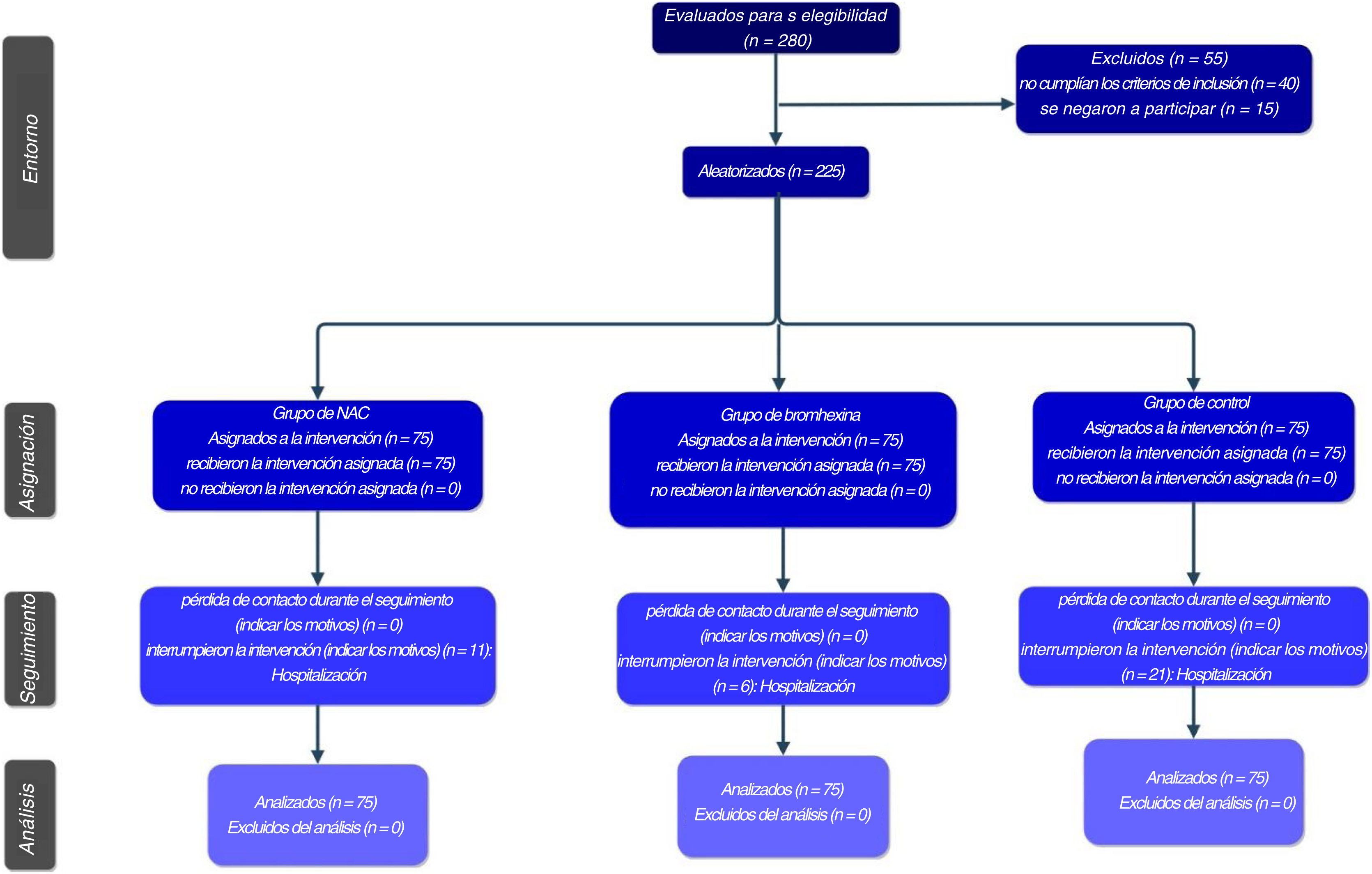
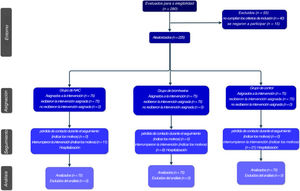
La cronología procedimental del estudio, representada mediante un diagrama de flujo Consort, permite definir la segmentación de los pacientes en función de los periodos de seguimiento posteriores hasta la conclusión de los resultados (fig. 2).
DiscusiónEn este estudio se investigó la eficacia de la NAC y la bromhexina en el tratamiento de pacientes con resultado positivo en la prueba de la COVID-19, y los resultados se compararon con un grupo de control que no había recibido ninguna medicación. En el estudio se incluyó a un total de 225 pacientes, asignados aleatoriamente a tres grupos. Los resultados del estudio indican que la tasa de hospitalización era menor tanto en el grupo de NAC como en el de bromhexina en comparación con el grupo de control, y se reducía la tasa de ingreso en la UCI. Aunque la diferencia no era estadísticamente significativa, el tiempo medio de hospitalización fue menor en los grupos de tratamiento en comparación con el grupo de control.
Además, nuestro estudio, junto con la investigación realizada por Izquierdo et al., indica que la NAC muestra resultados prometedores para la atenuación de la mortalidad de los pacientes y la reducción de los ingresos en la UCI durante el tratamiento de la COVID-1918. En el estudio dirigido por Milara et al. se examinó la activación del sistema de defensa del organismo conocido como inflamasoma en pacientes de COVID-19 gravemente enfermos, junto con el impacto mecanístico de la NAC en este proceso inflamatorio. Se recogieron pequeñas muestras de las vías respiratorias de los pacientes y se realizaron análisis genéticos y de proteínas. De este modo se demostró la mayor actividad del inflamasoma en los casos graves de COVID-19, observándose una activación aún mayor en la variante intensa. Los resultados indicaron que la NAC era capaz de mitigar la actividad del inflamasoma cuando se exponía al virus en un entorno de laboratorio. Esto sugiere una aplicación terapéutica prospectiva de la NAC en el tratamiento de los pacientes con COVID-1919. Asimismo, en un estudio realizado por Galindo-Andúgar et al. en 378 pacientes, de los cuales el 52,6% recibieron tratamiento con NAC, se concluyó que el tratamiento con este fármaco se identificaba como un factor protector frente a la mortalidad, lo que coincide con el resultado de nuestro estudio20. En otro estudio, realizado por Alam et al., en el que se llevó a cabo una revisión sistemática y un metaanálisis, se evaluó el efecto terapéutico del antioxidante NAC sobre la COVID-19. Analizando ocho estudios con 20 503 participantes, se encontró que el tratamiento con NAC se asociaba a una menor mortalidad en comparación con el grupo placebo (RR: 0,65). Además, la NAC daba lugar a reducciones significativas de los niveles de proteínaC reactiva (PCR) y dímeroD, así como a un aumento del marcador de oxigenación representado por el cociente PaO2/FiO2. A pesar del número limitado de estudios, los resultados sugieren un efecto positivo de la NAC en los resultados de la COVID-19, destacando la disminución de la mortalidad y las mejoras en los marcadores inflamatorios y la oxigenación21. Del mismo modo, el estudio realizado por Taher et al. respalda el efecto beneficioso de la NAC en el tratamiento de pacientes con COVID-1922. Además, la investigación realizada por Du Preez et al. aportó resultados coherentes con nuestro estudio, que demostraban el resultado positivo del uso de NAC23. Aunque estos estudios proporcionan resultados alentadores, es importante seguir explorando y validando la eficacia de la NAC como tratamiento para la COVID-19.
En un estudio realizado por Ansarin et al., que es similar a nuestra investigación, se concluyó que la bromhexina ha ayudado a mejorar significativamente los resultados clínicos, así como las tasas de mortalidad24. En otro estudio, realizado por Tolouian et al., se observó que el uso de bromhexina ayudaba a la recuperación de los pacientes con COVID-19, aunque, a diferencia de nuestro estudio, no tenía efecto sobre la mortalidad25.
En nuestro estudio, se observó que en todos los grupos las tasas de hospitalización y de mortalidad eran mayores en los hombres y entre la población de edad avanzada. Estos resultados concuerdan con el estudio realizado por Hesni et al. en Kermanshah17. Además, el tiempo medio de recuperación de los pacientes de los grupos de NAC y bromhexina era comparable, y ambos grupos mostraron un tiempo de recuperación más corto en comparación con el grupo de control. Sin embargo, la diferencia en el tiempo de recuperación no era estadísticamente significativa entre los grupos de tratamiento. En un estudio realizado por Tolouian et al. se observó que el uso de bromhexina resultaba útil para disminuir la duración de la hospitalización25.
En cuanto a los niveles de saturación de oxígeno, los resultados mostraron que la saturación media de oxígeno en los grupos de tratamiento era superior a la del grupo de control, sobre todo al séptimo día de la enfermedad. Los niveles medios de saturación de oxígeno también fueron comparables entre los grupos de NAC y de bromhexina.
La tasa de mortalidad entre los pacientes de los gruposA yB que recibieron la medicación fue nula, lo que coincide con los resultados de estudios anteriores, como la investigación de Ansarin et al.24. Sin embargo, la tasa de mortalidad en el grupo de control era significativamente superior en comparación con las cifras publicadas por el Johns Hopkins Coronavirus Resource Center26.
Una posible explicación de esta discrepancia es que en este estudio solo se incluyó a pacientes que no habían recibido vacunación para la COVID-19, lo cual representa un factor de riesgo conocido18. En este estudio se llevó a cabo una comparación entre la asociación de las enfermedades subyacentes y la COVID-19. Se observó que los pacientes hipertensos presentaban la tasa de mortalidad más elevada, con aproximadamente el 49% del total de fallecimientos. Este hallazgo concuerda con un estudio realizado por Javanmardi et al., en el que se notificó una tasa de mortalidad que oscilaba entre el 55% y el 37% entre los pacientes hipertensos, lo que respalda aún más nuestras observaciones. Además, en nuestro estudio se examinó la tasa de mortalidad de los pacientes con enfermedad cardiovascular, que se notificó como del 28,6%. Este resultado se asemeja bastante a las conclusiones de Javanmardi et al., quienes observaron una tasa de mortalidad similar que oscilaba entre el 16% y el 27% entre los pacientes con enfermedades cardiacas. Una posible explicación de la disparidad en las tasas de mortalidad entre dos grupos (grupoA y grupoB) y el grupoC podría atribuirse al hecho de que el tratamiento rápido y la detección precoz pueden contribuir significativamente a prevenir la mortalidad de los pacientes27.
Además, los resultados de este estudio indican que la NAC y la bromhexina pueden ser eficaces en el tratamiento de pacientes con resultado positivo en la prueba de la COVID-19. Estos tratamientos se asociaron a una menor tasa de hospitalización, un menor tiempo de hospitalización y una mejora de los niveles de saturación de oxígeno. En resumen, la detección precoz y el tratamiento rápido desempeñan un papel crucial en la reducción de las tasas de mortalidad. Además, las pruebas preliminares sugieren una posible eficacia de la NAC y la bromhexina en el tratamiento de los pacientes con COVID-19. Sin embargo, es importante señalar que son necesarios más estudios con un mayor tamaño de muestras y con períodos de seguimiento más largos para que podamos confirmar estos resultados.
ConclusionesEl presente estudio se llevó a cabo con el objetivo de investigar la eficacia de la NAC y la bromhexina en el tratamiento de pacientes con resultado positivo en la prueba de la COVID-19. Los resultados del estudio muestran que tanto el grupo de NAC como el de bromhexina presentaban una tasa de hospitalización inferior a la del grupo de control. Además, un porcentaje menor de pacientes requirieron ingreso en la UCI en los grupos de tratamiento. Aunque el uso de estos dos fármacos, bromhexina y NAC, no inducía cambios estadísticamente significativos en la tasa de hospitalización de los pacientes tanto con enfermedad subyacente como sin ella, sí era muy destacable su efecto en la tasa de mortalidad de las personas. No obstante, las enfermedades subyacentes siguen siendo los principales factores de riesgo. El tiempo medio de hospitalización en los grupos de tratamiento también fue menor que en el grupo de control. Además, el tiempo medio de mejora de los síntomas fue más corto en los grupos de NAC y bromhexina que en el grupo de control. Sin embargo, no se observaron diferencias estadísticamente significativas entre la NAC y la bromhexina en cuanto a la duración de la estancia hospitalaria o al tiempo transcurrido hasta la resolución de los síntomas.
En conclusión, los resultados de este estudio indican que la NAC y la bromhexina pueden ser eficaces para el tratamiento de pacientes con resultado positivo en la prueba de la COVID-19, con una menor tasa de hospitalización, una hospitalización más corta, un tiempo de recuperación más rápido y una reducción de la mortalidad en comparación con el grupo de control. No obstante, es necesario seguir explorando y validando la eficacia de la NAC y la bromhexina como tratamiento para la COVID-19, ya que estos resultados aportan evidencias alentadoras, aunque preliminares.
LimitacionesEn primer lugar, el estudio se realizó en un único centro médico de Irán con una población específica, y los hallazgos pueden no ser generalizables a otras poblaciones o entornos. En segundo lugar, se excluyó del estudio a los pacientes con enfermedades subyacentes, a los que precisaron hospitalización y a los que habían recibido vacunación para la COVID-19, lo que limitaba la generalización de los resultados a estos grupos específicos de pacientes. Finalmente, en estudios anteriores se habían identificado numerosos factores de riesgo de COVID-19, como las enfermedades subyacentes, la edad avanzada, la obesidad y la vacunación, entre otros. Este estudio se centró en algunos de estos factores, mientras que otros no pudieron ser investigados debido a conflictos con el contexto cultural del país.
Consideraciones éticasEste estudio fue aprobado por los Comités Éticos de Investigación de la Universidad de Ciencias Médicas de Hamadán, con el código ético IR.UMSHA.REC.1400.957. Además, fue aprobado por los árbitros del Centro Internacional de Registro de Ensayos Clínicos de Irán, miembro de los centros internacionales aprobados por la Organización Mundial de la Salud, con el código IRCT20220302054167N1, con fecha de registro 29-04-2022. Se obtuvo el consentimiento informado de todos los pacientes participantes en este estudio, o de sus tutores legales, tras explicarles detalladamente los métodos del estudio, los efectos secundarios de los fármacos y otras cuestiones necesarias de entender. Antes de participar, se examinaron los antecedentes de alergia a fármacos de todos los pacientes. Se les explicó detalladamente el estudio y se atendió a todas sus preguntas y dudas. También se recalcó a los pacientes que podían retirarse del estudio en cualquier momento sin que ello afectara a su tratamiento. Se les aseguró a todos ellos que su información personal sería confidencial y que solo se dispondría de la información colectiva de todo el estudio. Por último, todos los métodos se llevaron a cabo de acuerdo con las directrices y normativas pertinentes. Por lo tanto, la realización de la investigación se ajustó a los principios éticos de la Declaración de Helsinki.
FinanciaciónEste estudio ha contado con financiación interna.
AutoríaTodos los autores leyeron y aprobaron el manuscrito final.
Conflicto de interesesLos autores declaran que no tienen intereses económicos ni relaciones personales que pudieran haber influido en el trabajo presentado en este artículo.